Oxid uhliáitû§ a moéƒnosti jeho vyuéƒitûÙ I
fyzikûÀlnûÙ a chemickûˋ vlastnosti a jejich vyuéƒitûÙ v praxi
O oxidu uhliáitûˋm se v souáasnosti nejáastáji hovoéûÙ jako o obtûÙéƒnûˋm odpadu, kterûˋho je téeba se nájak zbavit. JednûÀ se péitom mnohdy o diskutabilnûÙ nûÀvrhy (napéûÙklad CCS) spojenûˋ s vysokû§mi nûÀklady a nejistû§m efektem. RacionûÀlnûÙ péûÙstup v duchu modernûÙch trendé₤ véÀak péedstavuje snaha o jeho materiûÀlovûˋ vyuéƒitûÙ. PrvnûÙ áûÀst álûÀnku péedstavuje zûÀkladnûÙ vlastnosti a péehled tradiánûÙch moéƒnostûÙ technickûˋho vyuéƒitûÙ oxidu uhliáitûˋho.
1. ûvod
Oxid uhliáitû§ je v souáasnûˋ dobá snad mediûÀlná nejznûÀmájéÀûÙm plynem. Zaslouéƒila se o to péedevéÀûÙm neustûÀle probûÙhajûÙcûÙ éƒivûÀ diskuse o zmánûÀch v klimatickûˋm systûˋmu Zemá, jejich péûÙáinûÀch, o skuteánû§ch i domnálû§ch nûÀsledcûÙch.
Na druhou stranu je téeba si uvádomit, éƒe oxid uhliáitû§ se svû§m aktuûÀlnûÙm objemovû§m obsahem zhruba 385 ppm v zemskûˋ atmosfûˋée umoéƒéuje éƒivot na Zemi v podobá, v jakûˋ jej znûÀme. Bez existence sklenûÙkovûˋho efektu, na náméƒ se podûÙlejûÙ i nákterûˋ daléÀûÙ plyny, by pré₤márnûÀ teplota byla péibliéƒná o 33 ô¯C niéƒéÀûÙ [1]. Oxid uhliáitû§ je souáûÀstûÙ péirozenû§ch péûÙrodnûÙch a biochemickû§ch cyklé₤ (kolobáh uhlûÙku, energetickûˋ procesy v éƒivû§ch organismech apod.). Je dobrûˋ mûÙt na památi, éƒe na uhlûÙku, resp. jeho organickû§ch slouáeninûÀch, je zaloéƒen veéÀkerû§ pozemskû§ éƒivot. Obsah oxidu uhliáitûˋho v atmosfûˋée se zûÀroveé jako jeden z celûˋ éady rozliánû§ch faktoré₤ podûÙlûÙ na ovlivéovûÀnûÙ vû§voje zemskûˋho klimatu.
Oxid uhliáitû§ je obsaéƒen péedevéÀûÙm v kouéovû§ch plynech z ré₤znû§ch druhé₤ spalovacûÙch procesé₤ a vznikûÀ rovnáéƒ jako odpad z éady chemickû§ch vû§rob (zpracovûÀnûÙ uhlûÙ, ropy, zemnûÙho plynu, vû§roba pûÀlenûˋho vûÀpna aj.) i z fermentaánûÙch procesé₤. ZûÀroveé unikûÀ do atmosfûˋry obrovskûˋ mnoéƒstvûÙ péi ré₤znû§ch biologickû§ch procesech v péûÙrodá, zpravidla véÀak v rozptû§lenûˋ formá.
O tomto plynu se v souáasnosti nejáastáji hovoéûÙ jako o obtûÙéƒnûˋm odpadu, kterûˋho je téeba se pouze nájak zbavit. JednûÀ se péitom mnohdy o diskutabilnûÙ nûÀvrhy spojenûˋ s vysokû§mi nûÀklady a nejistû§m efektem. RacionûÀlnûÙ péûÙstup v duchu modernûÙch trendé₤ véÀak péedstavuje snaha o jeho materiûÀlovûˋ vyuéƒitûÙ. ZajûÙmavûˋ fyzikûÀlnûÙ a chemickûˋ vlastnosti oxidu uhliáitûˋho jsou zûÀkladem pro ré₤znûˋ technickûˋ i chemickûˋ aplikace, kterûˋ naopak mohou péispát k ochraná éƒivotnûÙho prostéedûÙ, lidskûˋho zdravûÙ a do budoucna i û¤spoée ái nûÀhradá fosilnûÙch surovin. TéetûÙ moéƒnostûÙ je pak vyuéƒitûÙ v biologickû§ch kultivaánûÙch procesech (podpora fotosyntûˋzy). Péi û¤vahûÀch o moéƒnûˋm alternativnûÙm vyuéƒitûÙ oxidu uhliáitûˋho se sluéÀûÙ realisticky podotknout, éƒe celková vznikajûÙcûÙ mnoéƒstvûÙ tohoto plynu jsou tak obrovskûÀ, éƒe v ré₤znû§ch vû§éÀe zmûÙnánû§ch aplikacûÙch se mé₤éƒe uplatnit jen jeho relativná malûÀ áûÀst. JinûÀ situace v táchto relacûÙch by ovéÀem mohla nastat ve vzdûÀlenájéÀûÙ budoucnosti, kdy je nutno poáûÙtat s tûÙm, éƒe bude k dispozici jen oxid uhliáitû§ z biologickû§ch procesé₤ a spalovûÀnûÙ biomasy, péûÙp. doplnánû§ plynem zûÙskanû§m rozkladem uhliáitanovû§ch hornin nebo separovanû§m z atmosfûˋry.
2. FyzikûÀlnûÙ vlastnosti oxidu uhliáitûˋho
Oxid uhliáitû§ je za normûÀlnûÙch podmûÙnek bezbarvû§ plyn bez chuti a zûÀpachu. Od ostatnûÙch plyné₤, vyskytujûÙcûÙch se v atmosfûˋée, jej odliéÀujûÙ dvá vû§znamnûˋ vlastnosti [2]: trojnû§ bod (teplota 216,6 K, tlak 5,2 bar) a kritickû§ bod (teplota 314,12 K, tlak 73,75 bar). Vzhledem k vysokûˋmu tlaku trojnûˋho bodu nemé₤éƒe oxid uhliáitû§ existovat v kapalnûˋm stavu za tlaku atmosfûˋrickûˋho, mé₤éƒe bû§t pouze ve skupenstvûÙ plynnûˋm, nebo pevnûˋm (suchû§ led). KritickûÀ teplota je véÀak vyéÀéÀûÙ neéƒ teplota laboratornûÙ. Lze tedy oxid uhliáitû§ zkapalnit zvû§éÀenûÙm tlaku i za normûÀlnûÙch teplot. Péi teplotá péesahujûÙcûÙ teplotu kritickou nelze jiéƒ plyn stlaáenûÙm zkapalnit.
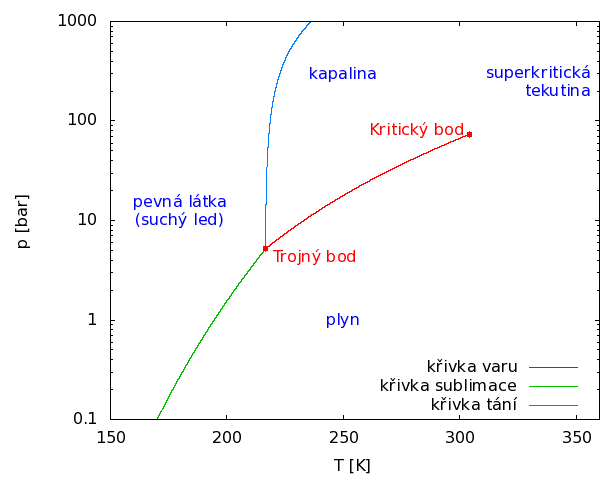
Obr. 1: FûÀzovû§ diagram oxidu uhliáitûˋho
Stlaáenûˋ tekutiny péi teplotá tásná nad teplotou kritickou vykazujûÙ anomûÀlnûÙ vlastnosti. Jejich transportnûÙ vlastnosti (viskozita, difuzivita) se blûÙéƒûÙ vlastnostem plyné₤, zatûÙmco hustota mûÀ hodnotu typickou pro kapaliny. ExtrakánûÙ schopnost takovûˋ tekutiny je vyéÀéÀûÙ neéƒ extrakánûÙ schopnost stejnûˋ lûÀtky v plynnûˋm stavu, v jednotce objemu se rozpustûÙ vátéÀûÙ mnoéƒstvûÙ. Vzhledem k vû§hodnájéÀûÙm transportnûÙm vlastnostem oxid uhliáitû§ snûÀze pronikûÀ do extrahovanûˋho materiûÀlu. Extrakce proto probûÙhûÀ rychleji. OddálenûÙ rozpuéÀtánûˋ lûÀtky od rozpouéÀtádla docûÙlûÙme snûÙéƒenûÙm tlaku. Extrakce se provûÀdájûÙ obvykle péi teplotûÀch od 30 do 60 ô¯C, takéƒe nedochûÀzûÙ k destrukci tepelná nestabilnûÙch lûÀtek.
3. Chemickûˋ vlastnosti oxidu uhliáitûˋho s péûÙklady klasickû§ch aplikacûÙ
Chemickûˋ reakce jsou v álûÀnku uvedeny pouze schematicky péedevéÀûÙm v sumûÀrnûÙ formá. Jednotlivûˋ dûÙláûÙ kroky jsou z dé₤vodu rozsahu textu dûÀle znûÀzornány jen vû§jimeáná. BliéƒéÀûÙ informace mohou zûÀjemci nalûˋzt v péûÙsluéÀnûˋ odbornûˋ literatuée.
Oxid uhliáitû§ se vyznaáuje lineûÀrnûÙ molekulou. Aákoli majûÙ kovalentná vûÀzanû§ uhlûÙk a kyslûÙk rozdûÙlnou elektronegativitu, molekula se nechovûÀ jako dipû°l, protoéƒe se parciûÀlnûÙ nûÀboje prûÀvá v dé₤sledku uvedenûˋ lineûÀrnûÙ struktury ruéÀûÙ.
Molekula vykazuje znaánou stabilitu. Teprve péi zûÀhéevu nad 2000 ô¯C se rozklûÀdûÀ na oxid uhelnatû§ a kyslûÙk:
Oxid uhliáitû§ je za normûÀlnûÙch podmûÙnek pomárná mûÀlo reaktivnûÙ plyn, kterû§ se tak áûÀsteáná podobûÀ jinû§m chemicky vûÙce ái mûˋná neteánû§m plyné₤m jako napé. dusûÙk nebo inertnûÙ plyny. Vû§jimku tvoéûÙ acidobazickûˋ reakce, kterûˋ majûÙ i áetnûˋ technickûˋ aplikace. Ve vodá se rozpouéÀtûÙ a vytvûÀéûÙ slabou nestabilnûÙ kyselinu uhliáitou, na kterou péipadûÀ péibliéƒná 0,2 % rozpuéÀtánûˋho plynu. Zbylû§ rozpuéÀtánû§ podûÙl se chovûÀ jako hydratovanû§ plyn. Z uvedenûˋho pohledu je vlastná oxid uhliáitû§ anhydridem kyseliny uhliáitûˋ.
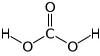
Kyselina uhliáitûÀ je dvojsytnûÀ a pomár jednotlivû§ch disociovanû§ch forem v roztoku zûÀvisûÙ na konkrûˋtnûÙch podmûÙnkûÀch (pH, teplota).
UkûÀzkou vyuéƒitûÙ acidobazickû§ch reakcûÙ oxidu uhliáitûˋho je po staletûÙ vyuéƒûÙvanû§ princip tuhnutûÙ vûÀpennûˋ malty, kterû§ lze vyjûÀdéit jednoduchou rovnicûÙ
Z modernûÙch aplikacûÙ lze uvûˋst napé. neutralizaci alkalickû§ch odpadnûÙch vod z pré₤myslu, kde oxid uhliáitû§ nahrazuje pouéƒitûÙ silnû§ch minerûÀlnûÙch kyselin. OdpadûÀ tak negativnûÙ efekt zasolenûÙ vod chloridy ái sûÙrany a eliminuje se nebezpeáûÙ péekyselenûÙ i rizika a komplikace péi manipulaci s kyselinami. Obdobnou reakci s roztoky alkalickû§ch hydroxidé₤, kterûÀ je zaloéƒena na chemickûˋ absorpci, lze vyuéƒûÙt k izolaci ze smási plyné₤.
Chemickûˋ vlastnosti oxidu uhliáitûˋho se v pré₤myslovûˋ praxi vyuéƒûÙvajûÙ péi znûÀmûˋ vû§robá sody Solvayovû§m postupem, jehoéƒ podstatu lze vyjûÀdéit sumûÀrnûÙ rovnicûÙ
Pré₤báh nákterû§ch reakcûÙ je téeba podpoéit vyéÀéÀûÙ teplotou a tlakem. PéûÙkladem je napé. vû§roba moáoviny, probûÙhajûÙcûÙ péi 230 ô¯C a tlaku 180 bar, schematicky znûÀzornánûÀ jako
Produkt se pouéƒûÙvûÀ péi vû§robá hnojiv, moáovino-formaldehydovû§ch pryskyéic, lûˋáiv i ve vû§robá kosmetickû§ch péûÙpravké₤ apod. Za zmûÙnku stojûÙ i pouéƒitûÙ k redukci oxidé₤ dusûÙku v kouéovû§ch plynech (metoda SNCR – Selective non catalytic reduction).
PéûÙkladem jinûˋ dé₤leéƒitûˋ pré₤myslovûˋ vû§roby je syntûˋza kyseliny salicylovûˋ (Kolbe-Schmittova syntûˋza, 120–140 ô¯C, 5–6 bar) sumûÀrná schematicky vyjûÀdéenûÀ nûÀsledovná:
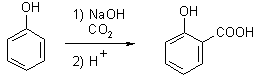
Produkt se nûÀsledná vyuéƒûÙvûÀ k vû§robá kyseliny acetylsalicylovûˋ, jednoho z nejpouéƒûÙvanájéÀûÙch lûˋáiv znûÀmûˋho pod ré₤znû§mi obchodnûÙmi nûÀzvy (aspirin, acylpyrin, aspro, upsarin apod.).
Z daléÀûÙch vû§rob v oblasti organickûˋ chemie je moéƒno zmûÙnit syntûˋzu cyklickû§ch karbonûÀté₤ reakcûÙ s epoxidy za souáasnûˋ katalû§zy (ethylen- a propylenkarbonat). Jsou pouéƒitelnûˋ pro daléÀûÙ syntûˋzy nebo jako rozpouéÀtádla péi vû§robá povlaké₤ ái jako elektrolyty v Li-iontovû§ch bateriûÙch. ExistujûÙ i péûÙklady syntûˋzy lineûÀrnûÙch polykarbonûÀté₤ s moéƒnostûÙ daléÀûÙho vû§raznájéÀûÙho rozvoje.
Za vysokû§ch teplot se oxid uhliáitû§ û¤áastnûÙ i oxidaáná-redukánûÙch reakcûÙ, kdy se chovûÀ jako slabûˋ oxidaánûÙ áinidlo. Reaguje tak napé. s alkalickû§mi kovy nebo kovy alkalickû§ch zemin:
Nejdé₤leéƒitájéÀûÙ reakcûÙ z tûˋto kategorie je vysokoteplotnûÙ redukce oxidu uhliáitûˋho uhlûÙkem, jak se uplatéuje zejmûˋna péi zplynovûÀnûÙ uhlûÙ a péi vû§robá éƒeleza ve vysokû§ch pecûÙch:
Znaáná specifickou katalytickou reakcûÙ, kde se oxid uhliáitû§ v nákterû§ch péûÙpadech uplatéuje, je syntûˋza methanolu. Jedna z obvyklû§ch technologiûÙ vychûÀzûÙ ze syntûˋznûÙho plynu (smás oxidu uhelnatûˋho a vodûÙku). Zde se buá oxid uhelnatû§ nahrazuje oxidem uhliáitû§m nebo se k vû§chozûÙ plynnûˋ smási péimûÙchûÀvûÀ oxid uhliáitû§ s vodûÙkem. TûÙmto postupem se ve svátovûˋm máéûÙtku vyrûÀbûÙ jen pomárná malûÀ áûÀst uvedenûˋho produktu:
Oxid uhliáitû§ mé₤éƒe takûˋ s vodûÙkem reagovat za podmûÙnek, kdy dochûÀzûÙ aéƒ k redukci na methan:
Tato tzv. Sabatierova reakce, kterûÀ probûÙhûÀ za vyéÀéÀûÙ teploty, tlaku a katalû§zy niklem (nováji s vyéÀéÀûÙ û¤áinnostûÙ rutheniem na oxidu hlinitûˋm), nabû§vûÀ v poslednûÙ dobá novûˋho vû§znamu v souvislosti s û¤vahami o akumulaci energie z obnovitelnû§ch zdrojé₤.
4. Fotosyntûˋza
Fotosyntûˋza mûÀ zûÀsadnûÙ vû§znam pro existenci vyéÀéÀûÙch forem éƒivota na Zemi. JednûÀ se o celû§ komplex redox reakcûÙ, kterû§ lze velmi zjednoduéÀená vyjûÀdéit sumûÀrnûÙ rovnicûÙ:
Za spolupé₤sobenûÙ sluneánûÙho zûÀéenûÙ a chlorofylu tak vznikajûÙ energeticky bohatûˋ slouáeniny. ûáinnost tohoto procesu je pomárná nûÙzkûÀ, ale jeho vû§znam je vzhledem k masovûˋmu vû§skytu v péûÙrodá obrovskû§. Je zûÀkladnûÙm kamenem kolobáhu uhlûÙku v péûÙrodá, péedpokladem produkce potravin a obnovitelnû§ch materiûÀlovû§ch i energetickû§ch zdrojé₤.
Jednotlivûˋ fûÀze fotosyntûˋzy jsou péedmátem vû§zkumu éady svátovû§ch vádeckû§ch pracoviéÀéË s ohledem na moéƒnûˋ budoucûÙ uplatnánûÙ v praxi. JednûÀ se napé. o chemickou aktivaci oxidu uhliáitûˋho spojenou s katalytickû§m éÀtápenûÙm tûˋto termodynamicky stabilnûÙ molekuly, kterûÀ je pak nûÀsledná schopna se zû¤áastnit éady reakcûÙ [3]. Tuto struánou zmûÙnku o fotosyntûˋze uvûÀdûÙme jen pro doplnánûÙ, i kdyéƒ s chemickû§mi aplikacemi oxidu uhliáitûˋho zdûÀnlivá péûÙmo nesouvisûÙ. Ve skuteánosti véÀak mé₤éƒe vû§hledová vû§zkum táchto katalytickû§ch mechanismé₤ otevéûÙt cestu k novûˋmu doposud neznûÀmûˋmu odvátvûÙ syntetickûˋ chemie.
5. Vybranûˋ technickûˋ aplikace
Oxid uhliáitû§ je vyuéƒûÙvûÀn v éadá procesé₤, kde se uplatéujûÙ jeho fyzikûÀlnûÙ a chemickûˋ vlastnosti. Jednou z typickû§ch aplikacûÙ je vysokotlakûÀ extrakce, aéË jiéƒ superkritickûÀ, nebo extrakce kapalnû§m oxidem uhliáitû§m péi teplotá mûÙrná podkritickûˋ. K oddálenûÙ rozpuéÀtánûˋ lûÀtky dochûÀzûÙ snûÙéƒenûÙm tlaku, vyhneme se tedy energeticky a áasová nûÀroánûˋ destilaci a suéÀenûÙ. Na druhou stranu je vysokotlakûˋ zaéûÙzenûÙ investiáná nûÀkladnûˋ. Vysokotlakûˋ extrakce tedy najdou uplatnánûÙ tam, kde lze vyuéƒûÙt jejich vû§hod. Jednou z oblastûÙ je potravinûÀéskû§ pré₤mysl, kde je nutno péi zpracovûÀnûÙ zachovat vitamûÙny a jinûˋ cennûˋ lûÀtky, kterûˋ jsou nestabilnûÙ péi vyéÀéÀûÙch teplotûÀch. DaléÀûÙ vû§hodou je nûÀhrada organickûˋho rozpouéÀtádla, kterûˋ mé₤éƒe péedstavovat zdravotnûÙ rizika, rozpouéÀtádlem netoxickû§m a velmi tákavû§m. Vzhledem ke stabilitá molekuly oxidu uhliáitûˋho nedochûÀzûÙ k chemickûˋ interakci s extrahovanû§mi lûÀtkami. Rozpustnost lûÀtek v tomto mûˋdiu je tedy uráena v podstatá bodem varu rozpouéÀtánûˋ lûÀtky, nikoliv jejûÙ polaritou. ExtrakánûÙ vlastnosti lze véÀak upravit péûÙdavkem malûˋho mnoéƒstvûÙ jinûˋho rozpouéÀtádla. V potravinûÀéskû§ch aplikacûÙch se pouéƒûÙvûÀ zejmûˋna voda a ethanol.
NejznûÀmájéÀûÙm procesem je extrakce chmele pro pouéƒitûÙ v pivovarnictvûÙ. Odhaduje se, éƒe tûÙmto postupem se zûÙskûÀvûÀ polovina svátovûˋ produkce chmelovûˋho extraktu. DaléÀûÙ aplikacûÙ je odstraéovûÀnûÙ kofeinu z kûÀvy a áaje. S vû§hodou se uvedenûÀ extrakce uplatéuje i péi zpracovûÀnûÙ daléÀûÙch péûÙrodnûÙch materiûÀlé₤, kdy se napé. z koéenûÙ a bylin zûÙskûÀvajûÙ aromatickûˋ lûÀtky, ûˋterickûˋ oleje apod.
Stéedem zûÀjmu je i vyuéƒitûÙ superkritickûˋ extrakce pro péûÙpravu krystalickûˋho oxidu titaniáitûˋho [4], depozici nanovrstev pro aplikace v mikroelektronice [5], péûÙpravu nanoáûÀstic β-karotenu [6]. Superkritickû§ oxid uhliáitû§ je tûˋéƒ studovûÀn jako prostéedûÙ pro homogenná katalyzovanûˋ reakce, napé. oxidaci celulû°zy [7], hydrogenaci styrenu [8] a lipûÀzou katalyzovanou syntûˋzu poly-L-laktidu [9].
Oxid uhliáitû§ se báéƒná pouéƒûÙvûÀ v nûÀpojovûˋm pré₤myslu nejen péi vû§robá sycenû§ch nûÀpojé₤, ale áasto takûˋ jako ochrannûÀ atmosfûˋra péi jejich péepravá a uchovûÀvûÀnûÙ v provoze i péi stûÀáenûÙ. Eliminuje se tak éÀkodlivûˋ pé₤sobenûÙ kyslûÙku, kterû§ nepéûÙznivá ovlivéuje senzorickou stabilitu a trvanlivost vû§robku.
Oxid uhliáitû§ se vyuéƒûÙvûÀ i péi áiéÀtánûÙ textiliûÙ. Protoéƒe textilie nejsou v kontaktu s organickû§m rozpouéÀtádlem, mé₤éƒe se jejich éƒivotnost prodlouéƒit o 30–40 %. Nákterûˋ evropskûˋ hotely jiéƒ nabûÙzejûÙ jako sluéƒbu hosté₤m áiéÀtánûÙ prûÀdla v takovû§ch áistûÙrnûÀch.
Impregnace déeva superkritickû§m oxidem uhliáitû§m nahrazuje vodnûˋ impregnaánûÙ roztoky i systûˋmy s organickû§mi rozpouéÀtádly. OdpadûÀ suéÀenûÙ a vû§hodou je i velkûÀ penetraánûÙ schopnost.
Oxid uhliáitû§ je pouéƒûÙvûÀn tûˋéƒ jako hnacûÙ plyn ve sprejûÙch. Nahrazuje chlorofluorovanûˋ uhlovodûÙky, kterûˋ poéÀkozujûÙ ozonovou vrstvu.
V neposlednûÙ éadá nachûÀzûÙ oxid uhliáitû§ uplatnánûÙ v hasicûÙch péûÙstrojûÙch. Jeho û¤áinek je kombinovanû§. Jednak ve formá snáhu (suchûˋho ledu) ochlazuje plamen, jednak vzhledem k tomu, éƒe je táéƒéÀûÙ neéƒ vzduch, vytvûÀéûÙ nad hoéûÙcûÙm péedmátem ochrannou atmosfûˋru, kterûÀ zabraéuje péûÙstupu kyslûÙku. Oxid uhliáitû§ je nevodivû§, lze jûÙm tedy hasit i elektrickûÀ zaéûÙzenûÙ pod proudem. Péi haéÀenûÙ nevznikajûÙ daléÀûÙ éÀkodlivûˋ lûÀtky a nezé₤stûÀvajûÙ rezidua jako péi pouéƒûÙvûÀnûÙ hasicûÙch péûÙstrojé₤ pánovû§ch ái prûÀéÀkovû§ch. Lze jej tedy pouéƒûÙt péi haéÀenûÙ poéƒûÀré₤ ve skladech potravin nebo v archivech, neboéË nedojde ke znehodnocenûÙ skladovanûˋho materiûÀlu a péedmáté₤, jeéƒ nebyly poéƒûÀrem zasaéƒeny.
ZajûÙmavou aplikacûÙ je áiéÀtánûÙ zneáiéÀtánû§ch povrché₤ tryskûÀnûÙm peletami suchûˋho ledu [10]. Pelety jsou na áiéÀtánû§ povrch unûÀéÀeny proudem stlaáenûˋho vzduchu. Povrch je áiéÀtán trojûÙm û¤áinkem: kinetickou energiûÙ pelet, ochlazenûÙm, jûÙméƒ je vrstva neáistot naruéÀena, a expanzûÙ péi sublimaci oxidu uhliáitûˋho. Odstranánûˋ neáistoty lze pak zamûˋst, nenûÙ nutno likvidovat rezidua rozpouéÀtádel.
Oxid uhliáitû§ je vyuéƒitelnû§ i jako chladicûÙ mûˋdium. Napé. v potravinûÀéstvûÙ se s vû§hodou pouéƒûÙvûÀ tzv. kryogennûÙ éÀokovûˋ zmrazovûÀnûÙ kapalnû§m oxidem uhliáitû§m, kterûˋ je velmi éÀetrnûˋ a dobée zachovûÀvûÀ vzhled i chuéË potravin po rozmrazenûÙ [11].
TepelnûÀ áerpadla s pracovnûÙ lûÀtkou oxidem uhliáitû§m se v praxi osvádáila nejáastáji k péûÙpravá teplûˋ vody péi vyuéƒitûÙ odpadnûÙho tepla, vhodnûˋ nasazenûÙ se nabûÙzûÙ u pré₤myslovû§ch suéÀicûÙch procesé₤ apod. [12]. ZajûÙmavûˋ je technickûˋ éeéÀenûÙ, kterûˋ je kombinacûÙ tepelnûˋ CO2-trubice jako hloubkovûˋ zemnûÙ sondy zkombinovanûˋ s tepelnû§m áerpadlem. TepelnûÀ trubice fungujûÙcûÙ jako vû§mánûÙk, kde probûÙhûÀ stûÀlûÀ cirkulace oxidu uhliáitûˋho na zûÀkladá samovolnûˋho odpaéovûÀnûÙ a kondenzace, péevûÀdûÙ z podzemûÙ teplo na povrch bez potéeby obáhovûˋho áerpadla. Na povrchu takto péivedenûˋ teplo vyuéƒûÙvûÀ tepelnûˋ áerpadlo s prománlivou frekvencûÙ otûÀáek kompresoru. Tato zaéûÙzenûÙ dosahujûÙ nadpré₤márnû§ch topnû§ch faktoré₤ a s tûÙm spojenûˋ vû§znamnûˋ û¤spory energie [13].
Currently carbon dioxide is commonly referred to as a difficult waste, which must be disposed in some way. The methods of disposal are often questionable (eg CCS) associated with high costs and uncertain effect. A rational approach in line with modern trends, however, is trying to use it as raw material. Overview of the technical possibilities of carbon dioxide utilization is presented.